Fe hóa trị mấy ? Khi nào Fe có hóa trị II và khi nào có hóa trị III là câu hỏi mà rất nhiều bạn thắc mắc. Bài viết này sẽ giúp bạn hiểu rõ hơn về hóa trị của sắt (Fe) trong hóa học.
Fe hóa trị mấy trong hóa học ?
Sắt (Fe) có hóa trị là +2 và +3, tùy thuộc vào phản ứng hóa học và điều kiện cụ thể.
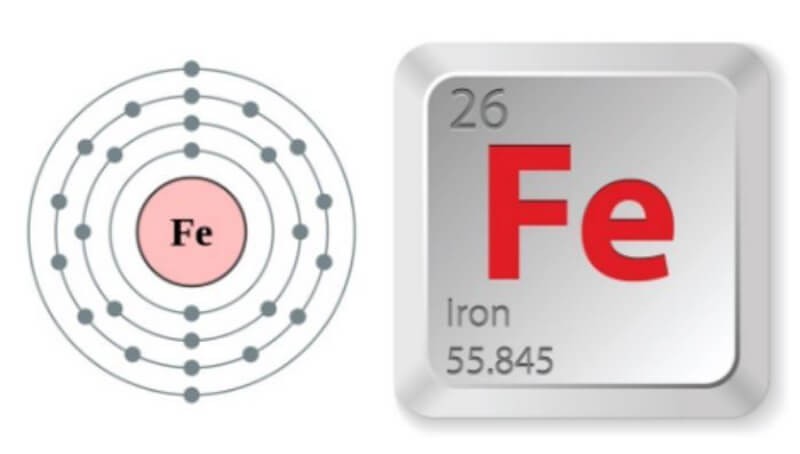
Tại sao sắt có hai hóa trị?
Để giải thích điều này, trước tiên cần xem xét cấu hình electron của sắt.
- Số hiệu nguyên tử của Fe là 26.
- Cấu hình electron đầy đủ: 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁶ 4s².
- Viết gọn : [Ar] 3d⁶ 4s².
Sắt thuộc chu kỳ 4, nhóm VIIIB trong bảng tuần hoàn.
Hóa trị của một nguyên tố là số lượng electron mà nguyên tố đó thu được hoặc mất đi hoặc chia sẻ để đạt được cấu hình electron bền của khí hiếm… Cũng lưu ý rằng quỹ đạo 3d có 1 cặp electron, các electron còn lại chưa ghép cặp. Bởi vậy, sắt thể hiện 2 trạng thái hóa trị là +2 và +3.
- Khi mất đi 2 electron 4s thì Fe có hóa trị +2.
- Đôi khi sắt cũng mất đi một trong các electron đã ghép cặp ở lớp 3d. Điều này khiến toàn bộ quỹ đạo 3d chứa đầy các electron chưa ghép cặp. Lúc này, hóa trị của sắt sẽ là +3.
Ví dụ của Fe theo hóa trị :
- Hóa trị +2: FeO, FeSO₄, Fe(OH)₂.
- Hóa trị +3: Fe₂O₃, Fe₂(SO₄)₃, Fe(OH)₃.
Như vậy, sắt có thể linh hoạt thay đổi hóa trị giữa +2 và +3 tùy vào điều kiện phản ứng, giúp nó tham gia vào nhiều hợp chất quan trọng trong hóa học và công nghiệp.
Xem thêm :Al hóa trị mấy ? Ứng dụng của nhôm trong cuộc sống
Khi nào Fe có hóa trị II và khi nào có hóa trị III?
Để hiểu rõ hơn về hóa trị của sắt trong các phản ứng hóa học, hãy cùng phân tích chi tiết dưới đây.

Khi nào Fe có hóa trị II?
Sắt thể hiện hóa trị II khi:
- Tác dụng với axit trung bình, tức là những axit mà gốc axit không có tính oxi hóa mạnh như HCl, H₂SO₄ loãng,…
- Phản ứng với dung dịch muối của kim loại yếu hơn, chẳng hạn như muối đồng, muối chì hoặc muối sắt (III).
- Khi tác dụng với phi kim hoạt động trung bình yếu cũng tạo ra muối Fe(II).
Tác dụng với axit trung bình:
- Fe + H₂SO₄ loãng → FeSO₄ + H₂
- Fe + 2HCl → FeCl₂ + H₂
Tác dụng với dung dịch muối của kim loại yếu hơn:
- Fe + Cu(NO₃)₂ → Fe(NO₃)₂ + Cu
- Fe + 2FeCl₃ → 3FeCl₂
Tác dụng với phi kim hoạt động trung bình yếu:
- Fe + S → FeS
Khi nào Fe có hóa trị III?
Sắt thể hiện hóa trị III khi:
- Phản ứng với axit có tính oxi hóa mạnh như HNO₃, H₂SO₄ đặc, nóng.
- Tác dụng với phi kim mạnh như F₂, Cl₂.
- Hợp chất sắt (II) bị oxi hóa bởi chất oxi hóa mạnh, chuyển thành hợp chất sắt (III).
Tác dụng với axit có tính oxi hóa mạnh:
- 2Fe + 6H₂SO₄ (đặc, nóng) → Fe₂(SO₄)₃ + 6H₂O + 3SO₂
Tác dụng với phi kim mạnh:
- 2Fe + 3Cl₂ → 2FeCl₃
Hợp chất sắt (II) bị oxi hóa thành sắt (III):
- 2FeCl₂ + Cl₂ → 2FeCl₃
- 2FeO + O₂ → 2Fe₂O₃
Xem thêm : Cl hóa trị mấy ? Ứng dụng của Cl trong cuộc sống



